Ang Tofacitinib citrate ay isang de-resetang gamot (trade name Xeljanz) na orihinal na binuo ng Pfizer para sa isang klase ng oral Janus kinase (JAK) inhibitors. Maaari nitong piliing pigilan ang JAK kinase, harangan ang mga daanan ng JAK/STAT, at sa gayon ay pigilan ang transduction ng signal ng cell at Related gene expression at activation, na ginagamit upang gamutin ang rheumatoid arthritis, psoriatic arthritis, ulcerative colitis at iba pang immune disease.
Ang gamot ay may kasamang tatlong mga form ng dosis: mga tablet, sustained-release na mga tablet at mga solusyon sa bibig. Ang mga tablet nito ay unang inaprubahan ng FDA noong 2012, at ang sustained-release dosage form ay inaprubahan ng FDA noong Pebrero 2016. Ito ang unang gumamot sa rheumatoid joints. Ang Yan ay isang JAK inhibitor na kinukuha nang pasalita isang beses sa isang araw. Noong Disyembre 2019, muling inaprubahan ang isang bagong indikasyon para sa mga sustained-release na gamot para sa moderate to severe active ulcerative colitis (UC). Bilang karagdagan, ang kasalukuyang phase 3 na klinikal na pagsubok para sa plaque psoriasis ay nakumpleto na, at isa pang anim na yugto 3 na klinikal na pagsubok ay isinasagawa, na kinasasangkutan ng aktibong psoriatic arthritis, juvenile idiopathic arthritis, atbp. Mga uri ng mga indikasyon. Ang mga bentahe ng mga sustained-release na tablet na matagal na kumikilos at kailangan lang inumin isang beses sa isang araw ay nakakatulong sa pamamahala at pagkontrol sa mga sakit ng mga pasyente.
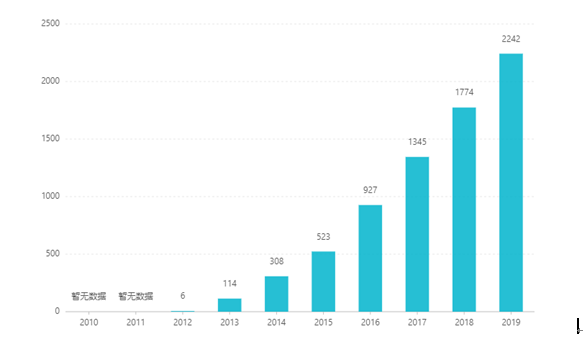
Mula nang ilista ito, tumaas ang mga benta nito taon-taon, na umaabot sa US$2.242 bilyon noong 2019. Sa China, ang tablet dosage form ay naaprubahan para sa marketing noong Marso 2017, at pumasok sa medical insurance category B catalog sa pamamagitan ng negosasyon noong 2019. Ang pinakabagong panalo ang bid ay RMB 26.79. Gayunpaman, dahil sa mataas na teknikal na mga hadlang ng mga paghahanda sa matagal na paglabas, ang form ng dosis na ito ay hindi pa naibebenta sa China.
Ang JAK kinase ay gumaganap ng isang mahalagang papel sa pamamaga, at ang mga inhibitor nito ay ipinakita upang gamutin ang ilang mga nagpapaalab at autoimmune na sakit. Hanggang ngayon, 7 JAK inhibitors ang naaprubahan sa buong mundo, kabilang ang Leo Pharma's Delgocitinib, Celgene's Fedratinib, AbbVie's upatinib, Astellas's Pefitinib, Eli Lilly's Baritinib At Novartis's Rocotinib. Gayunpaman, ang tofacitinib, baritinib at rocotinib lamang ang inaprubahan sa China sa mga nabanggit na gamot. Inaasahan namin ang "Tofatib Citrate Sustained Release Tablet" ng Qilu na maaprubahan sa lalong madaling panahon at makinabang sa mas maraming pasyente.
Sa China, ang orihinal na pananaliksik na tofacitib citrate ay inaprubahan ng NMPA noong Marso 2017 para sa paggamot sa mga pasyenteng may sapat na gulang na RA na may hindi sapat na bisa o hindi pagpaparaan sa methotrexate, sa ilalim ng trade name na Shangjie. Ayon sa data mula sa Meinenet, ang mga benta ng tofacitib citrate tablet sa mga pampublikong institusyong medikal ng China noong 2018 ay 8.34 milyong yuan, na mas mababa kaysa sa pandaigdigang benta nito. Ang isang malaking bahagi ng dahilan ay ang presyo. Iniulat na ang unang retail na presyo ng Shangjie ay 2085 yuan (5mg*28 tablets), at ang buwanang gastos ay 4170 yuan, na hindi isang maliit na pasanin para sa mga ordinaryong pamilya.
Gayunpaman, nararapat na ipagdiwang na ang tofacitib ay kasama sa 2019 “National Basic Medical Insurance, Work Injury Insurance at Maternity Insurance Drug List” ng National Medical Insurance Administration pagkatapos ng negosasyon noong Nobyembre 2019. Iniulat na mababawasan ang buwanang bayad hanggang sa ibaba 2,000 yuan pagkatapos mapag-usapan ang pagbawas sa presyo, na lubos na magpapahusay sa pagkakaroon ng gamot.
Noong Agosto 2018, ang Patent Reexamination Board ng State Intellectual Property Office ay gumawa ng desisyon sa pagsusuri No. 36902 na kahilingan para sa pagpapawalang-bisa, at idineklara na hindi wasto ang pangunahing patent ng Pfizertofatib, ang tambalang patent, sa mga batayan ng hindi sapat na pagsisiwalat ng detalye. Gayunpaman, ang patent ng Pfizertofatiib crystal form (ZL02823587.8, CN1325498C, application date 2002.11.25) ay mag-e-expire sa 2022.
Ipinapakita ng database ng Insight na, bilang karagdagan sa orihinal na pananaliksik, limang generic na gamot ng Chia Tai Tianqing, Qilu, Kelun, Yangtze River, at Nanjing Chia Tai Tianqing ang naaprubahan para sa marketing sa domestic tofacitinib tablet formulations. Gayunpaman, para sa sustained-release na uri ng tablet, tanging ang orihinal na pananaliksik na Pfizer ang nagsumite ng aplikasyon sa marketing noong Mayo 26. Ang Qilu ang unang domestic na kumpanya na nagsumite ng aplikasyon sa marketing para sa formulation na ito. Bilang karagdagan, ang CSPC Ouyi ay nasa yugto ng pagsubok ng BE.
Ang Changzhou Pharmaceutical Factory (CPF) ay isang nangungunang pharmaceutical manufacturer ng mga API, natapos ang mga formulation sa China, na matatagpuan sa Changzhou, Jiangsu province. Ang CPF ay itinatag noong 1949. Kami ay nakatuon sa Tofacitinib Citrate mula 2013, at nagsumite na ng DMF. Nakarehistro kami sa maraming bansa, at maaari kang suportahan ng pinakamahusay na suporta sa mga dokumento para sa Tofacitinib Citrate.
Oras ng post: Hul-23-2021